| Offizieller vollständiger Name |
Rekombinanter humaner Tumornekrosefaktor-alpha/TNFSF2 GMP (rHuTNF-alpha/TNFSF2) |
| Sequenz |
 |
| Aminosäuresequenz |
MVRSSSRTPS DKPVAHVVAN PQAEGQLQWL NRRANALLAN GVELRDNQLV VPSEGLYLIY SQVLFKGQGC PSTHVLLTHT ISRIAVSYQT KVNLLSAIKS PCQRETPEGA EAKPWYEPIY LGGVFQLEKG DRLSAEINRP DYLDFAESGQ VY |
| Synonyme |
Tumornekrosefaktor, TNFSF2, Cachectin, Differenzierungsfaktor, DIF, Necrosin, Cytotoxin |
| Zugangsnummer |
P01375 |
| GenID |
7124 |
| Zusammenfassung |
Tumornekrosefaktor alpha (TNF-alpha), auch Cachectin genannt, ist das bekannteste Mitglied der TNF-Familie, das zum Zelltod führen kann. Dieses Protein wird von Neutrophilen, aktivierten Lymphozyten, Makrophagen, NK-Zellen, LAK-Zellen, Astrozyten-Endothelzellen, glatten Muskelzellen und einigen transformierten Zellen produziert. TNF-alpha kommt als sezernierte, lösliche Form und als membranverankerte Form vor, die beide biologisch aktiv sind. Die natürlich vorkommende Form von TNF-alpha ist glykosyliert, aber nicht glykosyliertes rekombinantes TNF-alpha hat eine vergleichbare biologische Aktivität. Die biologisch aktive native Form von TNF-alpha ist angeblich ein Trimer. Humanes und murines TNF-alpha zeigen ungefähr 79 % Homologie auf Aminosäureebene und Kreuzreaktivität zwischen den beiden Spezies. Es wurden zwei Typen von Rezeptoren für TNF-alpha beschrieben und praktisch alle untersuchten Zelltypen zeigen das Vorhandensein eines oder beider dieser Rezeptortypen. |
| Quelle |
Escherichia coli. |
| Molekulargewicht |
Ungefähr 17.5 kDa, eine einzelne nicht-glykosylierte Polypeptidkette mit 158 Aminosäuren. |
| Biologische Aktivität |
Voll biologisch aktiv im Vergleich zum Standard. Die ED50, bestimmt durch einen Zytotoxizitätstest mit murinen L929-Zellen, beträgt weniger als 0.05 ng/ml, was einer spezifischen Aktivität von > 2.0 × 107 IE/mg in Gegenwart von Actinomycin D entspricht. |
| Optik |
Sterilfiltriertes weißes lyophilisiertes (gefriergetrocknetes) Pulver. |
| Formulierung |
Lyophilisiert aus einer 0.2 um filtrierten konzentrierten Lösung in 10 mM PB, 10 mM NaCl, pH 7.0. |
| Endotoxin |
Weniger als 0.01 EU/ug rHuTNF-α/TNFSF2 GMP, bestimmt nach der LAL-Methode. |
| Wiederherstellung |
Wir empfehlen, dieses Fläschchen vor dem Öffnen kurz zu zentrifugieren, um den Inhalt auf den Boden zu bringen. In sterilem destilliertem Wasser oder wässrigem Puffer mit 0.1 % BSA auf eine Konzentration von 0.1-1.0 mg/ml rekonstituieren. Stammlösungen sollten in Arbeitsaliquote aufgeteilt und bei ≤ -20 °C gelagert werden. Weitere Verdünnungen sollten in geeigneten Pufferlösungen erfolgen. |
| Stabilität und Lagerung |
Verwenden Sie einen manuellen Gefrierschrank und vermeiden Sie wiederholte Gefrier-Auftau-Zyklen.- Mindestens 12 Monate bei Lagerung bei ≤ -20 °C im Lieferzustand. Siehe chargenspezifisches COA für das Haltbarkeitsdatum.- 1 Monat, 2 bis 8 °C unter sterilen Bedingungen nach der Rekonstitution.- 3 Monate, -20 bis -70 °C unter sterilen Bedingungen nach der Rekonstitution. |
| Bibliographie |
1. Davenport C, Kenny H, Ashley DT, et al. 2012. Eur J Clin Invest, 42: 1173-9.2. Cavalcanti YV, Brelaz MC, Neves JK, et al. 2012. Pulm Med, 2012: 745483.3. Sheng WS, Hu S, Ni HT, et al. 2005. J Leukoc Biol, 78: 1233-41.4. Berthold-Losleben MandHimmerich H. 2008. Curr Neuropharmacol, 6: 193-202. |
| SDS-SEITE |
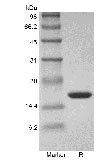 |
| Sicherheitsdatenblatt (SDB) herunterladen |
Zum Herunterladen klicken |
| Technisches Datenblatt (TDS) herunterladen |
Zum Herunterladen klicken |



